Boletín Oficial
ANMAT prohibió el uso y comercialización de bombas de infusión extraviadas
:format(webp):quality(40)/https://sur24cdn.eleco.com.ar/media/2026/02/bombas_de_infusion.webp)
La medida alcanza a equipos de riesgo III registrados por la firma ICU Medical Argentina. Se trata de unidades específicas cuyos números de serie fueron detallados oficialmente.
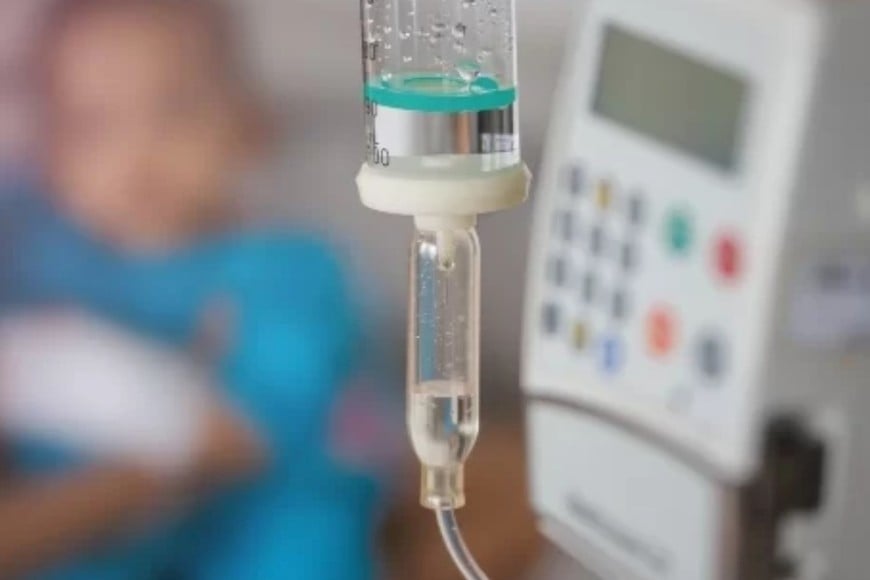
La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) dispuso la prohibición del uso, comercialización y distribución en todo el país de determinadas bombas de infusión de las marcas Plum A+TM y Plum360TM, luego de que la empresa titular informara el extravío de varias unidades. La decisión quedó formalizada a través de la Disposición 259/2026, publicada en el Boletín Oficial.
Según consta en el texto oficial, la medida se originó a partir de una notificación realizada por la firma ICU Medical Argentina S.R.L., habilitada como importadora de productos médicos bajo el Legajo N° 2028. La empresa comunicó el extravío de equipos identificados con números de serie específicos y presentó la correspondiente denuncia ante el Gobierno de la Provincia de Buenos Aires.
Qué equipos están alcanzados por la prohibición
La disposición detalla que la prohibición alcanza a las siguientes unidades:
Bomba de infusión Plum A+TM (PM 2028-22), números de serie: 18314614, 18313908, 18311337, 18313170, 18312661, 18302456 y 18301723.
Bomba de infusión Plum360TM (PM 2028-45), número de serie: 20852391.
Se trata de productos médicos clasificados como de riesgo III, es decir, dispositivos que cumplen funciones críticas en la atención sanitaria y cuyo uso indebido o en condiciones no verificadas puede implicar riesgos significativos para los pacientes.
Puede interesarte
De acuerdo con la documentación oficial, la bomba Plum A+TM está indicada para proporcionar infusiones por vía parenteral, enteral o epidural, mientras que la Plum360TM se utiliza para terapias parenterales, enterales y epidurales, además de la administración de sangre o productos sanguíneos.
Al tratarse de equipos destinados a la administración controlada de medicamentos y fluidos en pacientes, su trazabilidad y estado técnico resultan fundamentales para garantizar la seguridad en hospitales, clínicas y otros establecimientos de salud.
El motivo de la medida y su alcance
La ANMAT fundamentó la decisión en la necesidad de “proteger a eventuales adquirentes y usuarios” de los productos involucrados, dado que se trata de unidades individualizadas cuyo estado y condición se desconocen tras su extravío
En este sentido, el organismo resolvió prohibir su uso, comercialización y distribución en todo el territorio nacional. La disposición establece en su artículo 1° la prohibición expresa sobre los equipos mencionados y ordena en el artículo 2° su publicación en el Boletín Oficial, así como la comunicación a las autoridades sanitarias provinciales y de la Ciudad Autónoma de Buenos Aires
Además, se dio intervención a la Dirección de Evaluación y Gestión de Monitoreo de Productos para la Salud y a la Coordinación de Sumarios, en el marco de las facultades conferidas por el Decreto N° 1490/92 y sus modificatorias, normativa que regula las competencias del organismo.
La disposición lleva la firma del administrador nacional, Luis Eduardo Fontana, y fue publicada con fecha 13 de febrero de 2026 en el Boletín Oficial
Por qué es clave la trazabilidad en productos médicos
Las bombas de infusión son dispositivos ampliamente utilizados en unidades de terapia intensiva, servicios de oncología, neonatología y en internaciones generales, donde permiten administrar fármacos, soluciones y hemoderivados de manera controlada y precisa.
Al ser equipos electrónicos programables, requieren controles técnicos, mantenimiento periódico y verificación de su correcto funcionamiento. Cuando una unidad se extravía y pierde su circuito formal de distribución y control, las autoridades sanitarias no pueden garantizar que se conserve en condiciones adecuadas ni que no haya sido manipulada.
Por eso, ante la pérdida de dispositivos de riesgo III, la normativa prevé la adopción de medidas preventivas como la prohibición de uso, incluso cuando no se hayan reportado incidentes. El objetivo es evitar que esos equipos reaparezcan en el mercado informal o sean utilizados sin las garantías correspondientes.
Desde el punto de vista sanitario, la decisión apunta a reducir cualquier posibilidad de daño derivado de un funcionamiento defectuoso, calibración incorrecta o alteración de componentes internos.
Puede interesarte
Qué deben tener en cuenta las instituciones de salud
La disposición no implica un retiro general del mercado de las líneas Plum A+TM o Plum360TM, sino que se limita estrictamente a las unidades cuyos números de serie fueron detallados. Es decir, otros equipos de la misma marca y modelo que no coincidan con esos identificadores pueden continuar en uso, siempre que cuenten con la documentación y habilitación correspondientes.
En caso de que alguna institución o profesional detecte la presencia de una de las bombas incluidas en la prohibición, deberá abstenerse de utilizarla y dar aviso a la autoridad sanitaria competente.
La publicación oficial también ordena la comunicación a las autoridades sanitarias provinciales y de la Ciudad Autónoma de Buenos Aires, a fin de reforzar la difusión de la medida y facilitar su cumplimiento en todo el país.

